L'estérification et l'hydrolyse en terminales S ! |
||||||||
 @ Me contacter |
Accueil | Le cours | Les exercices | |||||
|---|---|---|---|---|---|---|---|---|
L'estérification et l'hydrolyse en terminales S ! |
||||||||
 @ Me contacter |
Accueil | Le cours | Les exercices | |||||
|---|---|---|---|---|---|---|---|---|
Fiche de cours de chimie
Terminale S
Lorsqu'on mélange un alcool et un acide carboxylique, il se forme un ester: c'est la réaction d'estérification.
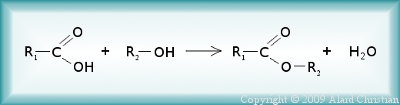
Lorsqu'on mélange un ester avec de l'eau, il se forme un alcool et un acide carboxylique: c'est la réaction d'hydrolyse.
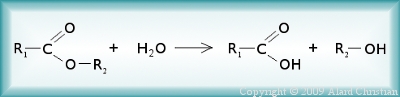
Les réactions d'estérification et d'hydrolyse sont inverses l'une de l'autre. Ces deux réactions sont lentes, limitées et ne dégage pas de chaleur.
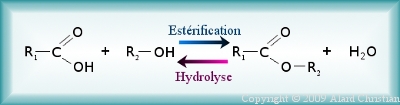
Pour nommer un ester, il faut repérer l'acide et l'acool ayant servi à sa formation, puis il faut donner le nom de l'acide et remplacer la terminaison « -oïque » par « -oate » et nommer à la suite le groupement alkyle correspondant à l'alcool.
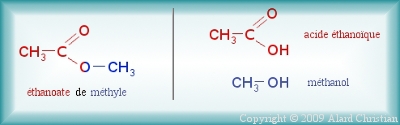
Pour une espèce chimique synthétisée, le rendement de la réaction de synthèse correspond au rapport suivant:
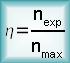

Les rendements des réactions d'estérification et d'hydrolyse dépendent de la classe des alcools mis en jeu. Plus la classe de l'alcool est grande, plus la réaction est favorisée dans le sens de l'hydrolyse.
Lors du calcul du quotient réactionnel, il faut prendre en compte la concentration de l'eau dans le milieu réactionnel car elle ne joue pas ici le rôle de solvant (contrairement aux réactions acido-basiques).


L'augmentation de la température de réaction ou l'utilisation d'un catalyseur n'augmente en rien le rendement de la réaction mais permet d'atteindre plus vite l'état d'équilibre.
L'utilisation d'un anhydride d'acide plutôt que d'un acide carboxylique rend la réaction d'estérification totale, rapide et exoenergétique.
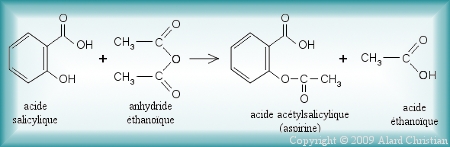
L'estérification de l'acide salicilique à l'aide de l'anhydride éthanoïque correspond à la synthèse de l'aspirine.
L'utilisation d'ions hydroxyde plutôt que de l'eau rend la réaction d'hydrolyse totale et rapide.
L'hydrolyse des triesters du glycérol (triglycérides) à l'aide d'hydroxyde de sodium est appelée réaction de saponification et correspond à la réaction de synthèse des savons selon la réaction suivante:
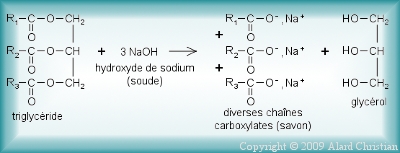
Les chaîne carboxylates issues de la saponification de triglycéride correspondent à de longues chaines carbonnées (partie lipophile ou hydrophobe) rattachée au groupement carboxylate (partie hydrophile ou lipophobe). C'est cette structure particulière qui confère ses propriétés nettoyantes au savon (formation de micelles).